Убедить пациентку в отсутствии у нее настоящей тромбофилии бывает непросто. То ли термин звучит благородно и не хочется расставаться с мыслью, что такого «красивого» диагноза у нее все-таки нет, то ли до меня другой доктор слишком красочно убеждал в обратном… Так или иначе, но путаницу с терминологией необходимо устранять, поскольку именно от наличия или отсутствия истинной тромбофилии зачастую зависит тактика ведения беременности или лечения после тромбоза.
Почему диагноз встречается так часто
Еще буквально лет шесть назад результаты обследования на предмет носительства генетических полиморфизмов, располагающих к тромбозам, интерпретировали примерно так: за каждый полиморфизм присваивалось определенное количество баллов. Баллы суммировались и, в зависимости от их количества, результат попадал в одну из трех градаций: тромбофилия высокого риска, тромбофилия умеренного риска, тромбофилия низкого риска. Практически только ноль баллов исключал возможность поставить диагноз «тромбофилия» (а таких людей, у которых из 7-12 исследованных генов ни в одном нет полиморфизма, я лично встречала раза 3-4 за все годы работы). И с тех, сравнительно недавних еще пор огромное количество пациенток убеждены в том, что у них тромбофилия, и, приходя наблюдать следующую беременность, сообщают об этом врачу. Врач, естественно, такую информацию игнорировать не может, и диагноз бережно переносится уже в новую диспансерную книжку…
У кого же она есть?
К счастью, достаточно быстро в научной среде были расставлены точки над i, определение и критерии тромбофилии в настоящее время закреплены в клинических рекомендациях (как общих, так и акушерских), и специалисты ставят данный диагноз только в строго определенных случаях.
К истинным тромбофилиям относятся только следующие состояния:
-
дефицит антитромбина;
-
дефицит протеина С и (или) протеина S;
-
резистентность к активированному протеину С (АРС-резистентность);
-
антифосфолипидный синдром;
-
высокий уровень гомоцистеина крови;
-
наличие мутации Лейден в факторе 5;
-
наличие мутации в гене протромбина G20210A.
Согласно определению ВОЗ, для людей, имеющих тромбофилию, характерна такая склонность к тромбообразованию, которая существенно отличает их от других людей. Эти отличия – в более раннем возрасте начала тромбозов, повторяющихся эпизодах тромбозов; нередко родственники пациентов также переносили тромбозы (семейная история). Причем спровоцировать тромбоз у людей с тромбофилией может фактор, незначительный по своей силе для других людей. Другими словами, далеко не у всех ведь случаются тромбозы после родов, авиаперелетов, ношения гипса на сломанной ноге или, скажем, приема оральных контрацептивов? А для пациентов с тромбофилией в этих ситуациях риск выше в десятки раз.
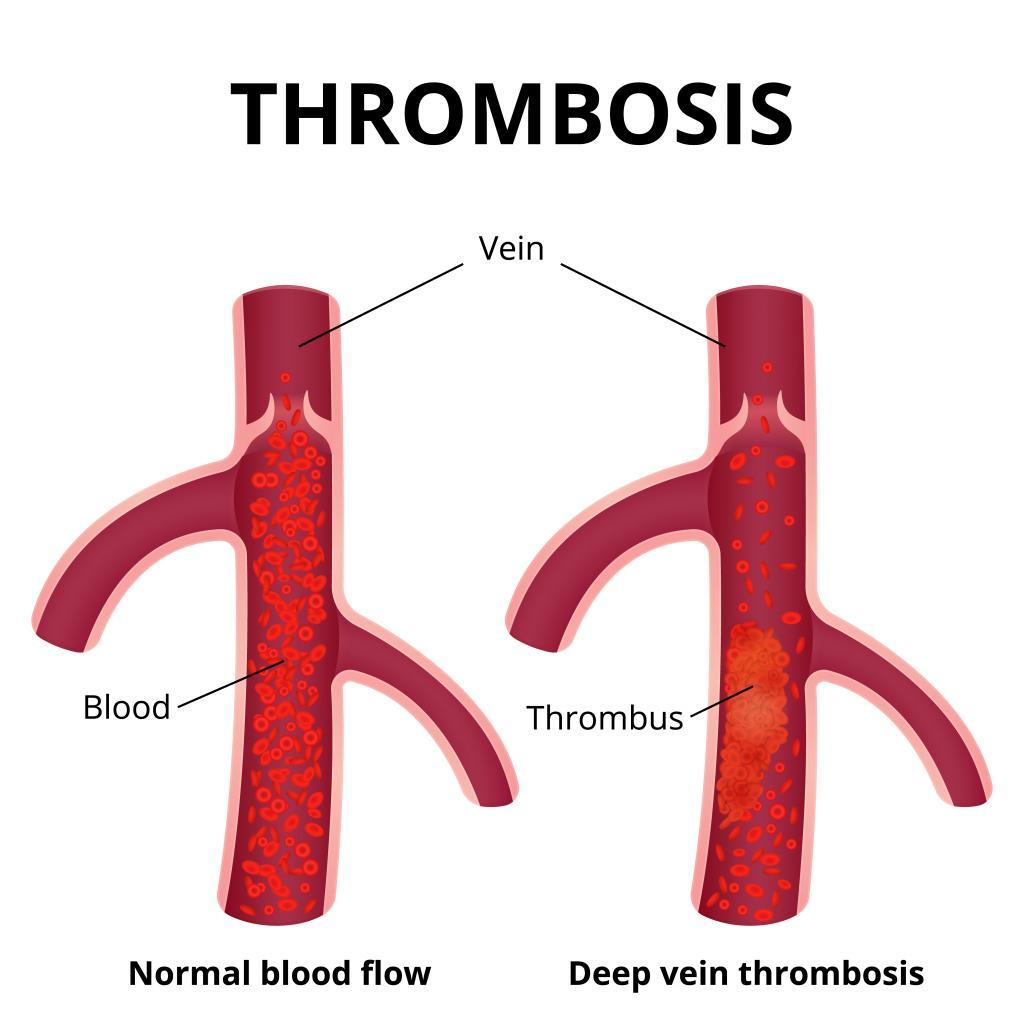
Источник фото:
Чуть подробнее о каждом
Носительство мутаций (последние два пункта в списке) – факт, не подлежащий изменениям, то есть с мутацией Лейден, например, человек рождается и живет всю жизнь, передавая с определенной долей вероятности ее и своим детям. Вероятность передачи зависит от типа носительства: гомозиготное или гетерозиготное. Гомозигота – когда в паре одноименных генов, полученных нами от наших родителей, оба гена с мутацией. Гетерозигота – когда только один родитель передал нам ген с мутацией, а от второго пришел здоровый ген. Нетрудно догадаться, что гомозиготное носительство более опасно, так как «хромают обе ноги» в геноме и нет хотя бы одного здорового гена, который работал бы нормально. Гомозиготный носитель передаст ген с мутацией всем своим детям, то есть дети будут как минимум гетерозиготными носителями. А вот гетерозиготный носитель передаст мутированный ген детям с вероятностью 50%, ведь у него есть второй здоровый ген, который с такой же вероятностью может занять место в половой клетке.
Дефицит антитромбина, протеина С или протеина S – это состояние, когда ослабевает естественная защита организма от избыточного тромбообразования, ведь эти три белка являются самыми важными природными антикоагулянтами. Снижение количества любого из них ниже определенных значений существенно повышает риск тромбозов и акушерских осложнений.
Антифосфолипидному синдрому посвящена отдельная статья. Заметим лишь, что, в отличие от наследственных тромбофилий (мутаций и дефицитов антикоагулянтов), АФС относится к приобретенным нарушениям гемостаза. Патологические антитела, за счет которых реализуются все осложнения при АФС, могут появляться внезапно в любой период жизни и, что примечательно, могут так же внезапно исчезать. Поэтому диагноз АФС не пожизненный, он может быть снят в том случае, если антитела не определяются в крови более 5 лет и за это время не случилось новых тромбозов или потерь беременности.
Все вышеперечисленные состояния требуют обязательного наблюдения гемостазиолога во время беременности и непрерывного лечения разжижающими препаратами вплоть до родов и еще как минимум 42 дня после них. Исключением является гетерозиготное носительство мутаций Лейден и гена протромбина, когда непрерывный курс лечения требуется не в 100%, а в зависимости от клинической ситуации, по решению врача.
А вот высокий уровень гомоцистеина (гипергомоцистеинемия) – состояние куда менее трагичное. Гомоцистеин повышается в тех случаях, когда организм испытывает дефицит фолиевой кислоты. Примечательно, что дефицит может сохраняться даже при употреблении препаратов фолиевой кислоты в связи с индивидуальными особенностями обмена веществ. Гомоцистеин в высоких концентрациях обладает различными неблагоприятными эффектами: повышает активность тромбообразования, способствует гибели клеток трофобласта (зачаточной плаценты) на ранних сроках беременности, повышает риск развития плацентарных осложнений – преэклампсии, отслойки плаценты, артериальной гипертензии.
При выявлении повышенного гомоцистеина снизить его обычно не проблема. Существуют различные схемы и препараты, выбор в каждом случае индивидуален. Ответ на лечение тоже может варьировать: у кого-то показатель снижается до нормы за месяц, а кому-то требуется несколько месяцев и сочетание разных препаратов, но в конечном итоге еще ни разу мы с пациентами не проигрывали эту битву! Очень важно определить уровень гомоцистеина до беременности и снизить его заблаговременно, ведь если этого не сделать, можно упустить самые важные первые недели, когда как раз максимально проявляются пагубные эффекты гипергомоцистеинемии.
Важно: нормы лабораторий не распространяются на беременных! Безопасным для 1-го триместра считается уровень гомоцистеина ниже 8 мкмоль/л.
Д-димер и тромбофилия
Сам по себе высокий Д-димер, так же как и отклонения любых показателей гемостазиограммы, не является показанием для лечения. Поэтому стремиться снизить его до нормы не нужно, да это и вряд ли получится. Лечение назначается только в том случае, если имеются реальные факторы риска, связанные с заболеваниями, тяжелым анамнезом или наличием подтвержденной тромбофилии. Он может быть абсолютно нормальным при тяжелой тромбофилии, а может быть сильно повышен у здоровых женщин во время беременности. Поэтому решение принимается не по результату анализа, а по совокупности данных.
После стимуляции овуляции Д-димер действительно может повышаться до нескольких тысяч. И здесь лечение оправдано, потому что в протоколе ЭКО такие цифры Д-димера говорят, скорее всего, о наличии синдрома гиперстимуляции яичников. Это состояние бывает разной степени тяжести, при средней и тяжелой степени лечение разжижающими препаратами продолжается как минимум 3 месяца. Однако и при легкой степени синдрома лечение может быть длительным, это зависит от течения беременности и сопутствующих факторов риска. Решение о продолжительности курса каждый раз принимается индивидуально.

Источник фото:
Что сюда не относится?
Ну и что же в итоге осталось за кадром? – Все остальные генетические полиморфизмы, которые, в принципе, можно и не определять: FGB, ITG A2, ITG B3, F13, F VII, PAI-1 (SERPINE)… Разве что последний, PAI-1, при гомозиготном носительстве может насторожить врача, когда речь идет о невынашивании беременности. Но по большому счету существенно на тактику лечения его наличие или отсутствие влиять не должно.
Все полиморфизмы, начинающиеся на MT – MTHFR, MTRR, MTR – относятся к системе генов, кодирующих обмен гомоцистеина. По сути, это маркеры генетической предрасположенности к гипергомоцистеинемии, которая может реализоваться у данного пациента в течение жизни, а может и нет. Определять их совершенно необязательно, куда информативнее просто сдать анализ на гомоцистеин и получить объективную информацию о том, повышен он или нет.
Резюме
Надеюсь, большая часть читательниц, сдававших когда-либо анализ на генетические тромбофилии, сейчас выдохнули с облегчением и порадовались, что тромбофилии у них нет. Но помним, что обследование на тромбофилию включает не только генетический анализ. И, кроме того, разумеется, если случаи потери беременности продолжаются, при планировании следующей необходимо проконсультироваться с гемостазиологом. Ведь наши знания не безграничны, как и возможности лабораторий. И далеко не всегда отрицательный анализ означает полное отсутствие угрозы.


























При добавлении нового комментария на данный материал, Вам на почту будет приходить уведомление об этом со ссылкой на новый комментарий. В любой момент Вы можете отписаться от уведомлений, перейдя по специальной ссылке в тексте письма.
Для активации подписки, просьба перейти по ссылке в письме!
В смысле не верят? Люди какие то странные....
Действительно, странные люди: не хотят верить в то, что они здоровы)))
Обычно это бывает у тех, кто очень любит страдать
Новый уровень страдания: искать тромбофилию